作者简介:曹兴(1984—),男,山东滕州人,博士,讲师,主要从事园艺作物病害防治研究。E-mail: caoxinglina@163.com
转录辅激活因子MBF1a参与了植物对病原真菌的防御反应。利用电子克隆结合RT-PCR技术从百合中分离了 LlMBF1 a基因,其开放阅读框长429 bp,编码142个氨基酸。LlMBF1a分子量为15.53 ku,理论等电点为10.12,为稳定的水溶性非分泌蛋白,含有典型的MBF1结构域和α螺旋-转角-α螺旋模序。亚细胞定位分析表明,LlMBF1a主要在细胞核中表达。 LlMBF1 a在根、茎、鳞茎、叶中的表达量无显著差异,受灰葡萄孢菌侵染诱导表达且在相对抗病品种中持续高水平表达,表明 LlMBF1 a可能参与了百合对灰霉病的抗性反应。
Previous studies revealed that MBF1a was involved in host defense response. The MBF1 a homologous gene was isolated from lily cultivar White Heaven by silico cloning and RT-PCR approaches. The open reading frame of LlMBF1 a gene was 429 bp, encoding a protein of 142 amino acid residues, and the molecular weight of LlMBF1a protein was 15.53 ku with a theoretical isoelectric point of 10.12. Bioinformatics analysis predicted that LlMBF1a was a stable soluble non-secreted protein, containing a typical MBF1 motif and a helix-turn-helix motif. Subcellular localization assay indicated LlMBF1a expressed in nucleus. The expression of LlMBF1 a was at a similar level in leaf, stem, bulb and root, and was induced by Botrytis cinerea. The up-regulation of LlMBF1 a in resistant variety was higher and more persistent than that in susceptible variety, suggesting LlMBF1 a might be correlated to the resistance of lily against gray mold.
百合(Lilium spp.)为百合科百合属球根花卉, 具有重要的观赏、食药用价值。百合灰霉病是百合的主要病害之一, 主要为害百合的叶、茎和花, 导致叶片枯死、花器褐腐、茎秆发黑和鳞茎停止生长, 严重影响百合的产量和质量, 制约了百合商品化周年生产[1]。培育抗病品种是防治灰霉病的有效途径, 而解析百合与病原菌互作的分子机制是百合灰霉病抗性遗传改良的基础。植物多蛋白桥梁因子(multiprotein bridging factor 1, MBF1)又称转录辅激活因子(transcriptional co-activator), 可以连接通用转录因子TBP(TATA-box binding protein)和基因特异性转录因子, 从而增强特异性转录因子的DNA结合活性, 最终促进靶基因的表达[2], 如WRKY、CBF、MAPK3/11和钙结合蛋白等。研究表明, MBF1参与了植物的病原真菌胁迫反应。小麦TaMBF1a[3]、拟南芥AtMBF1a[4]、马铃薯StMBF1[5]的表达均受真菌侵染诱导, 拟南芥过表达AtMBF1a的转基因植株, 提高了对灰葡萄孢菌(Botrytis cinerea)的抗性[4]。
目前, 关于百合MBF1的研究尚未见报道。我们从麝香百合(Lilium longiflorum)成熟花粉EST数据库中筛选了一个MBF1同源基因LlMBF1a, 分析了该基因的表达模式及该蛋白的特征, 以期为进一步研究LlMBF1a基因在百合灰霉病抗性反应中的功能及作用机制提供理论参考。
试验材料为麝香百合杂种系(Lilium longiflorum hybrids)品种白天堂(White Heaven)和粉红珍珠(Pink Pearl), 栽培基质为蛭石+草炭(体积比1∶ 1), 培养温度为22 ℃, 光照时间为16 h· d-1。亚细胞定位使用的材料为本氏烟(Nicotiana benthamiana)。百合灰霉病病原物灰葡萄孢菌(Botrytis cinerea)由本实验室分离、纯化并保存。
RNA提取试剂盒、大肠埃希菌感受态DH5α 购自北京天根生化科技有限公司; DNA片段回收试剂盒、质粒提取试剂盒购自北京百泰克生物技术有限公司; pMD18-T载体、M-MLV逆转录试剂盒、PrimeSTAR HS DNA聚合酶、T4连接酶、限制性内切酶(SalⅠ 、SpeⅠ 、SmaⅠ )、荧光定量试剂盒SYBR® Premix Ex TaqTM Ⅱ (Tli RNaseH Plus)等购自TaKaRa公司; 氨苄青霉素(Amp)、卡那霉素(Kan)购自Sigma公司; 其他常规试剂均为进口或国产分析纯; 引物由生工生物工程(上海)股份有限公司合成(表1); DNA测序由北京六合华大基因科技有限公司完成; 亚细胞定位载体pCAMBIA1300由中国农业大学花卉发育与品质调控北京市重点实验室惠赠。
| 表1 逆转录和PCR引物 Table 1 Primers applied in PCR |
1.2.1 LlMBF1a cDNA序列的克隆
取0.1 g白天堂叶片用液氮研磨提取RNA。RNA的提取和cDNA的合成参照隋娟娟等[6]的方法。根据NCBI上已报道的拟南芥(Arabidopsis thaliana)AtMBF1a的mRNA序列, 利用BLAST程序搜索与其高度相似的百合表达序列标签(expressed sequence tag, EST)。然后将该序列(BP176978)在NCBI上进行同源比对, 用ORF Finder程序预测其开放阅读框(open reading frame, ORF)。在起始密码子上游设计特异引物SPF1, 在终止密码子下游设计特异引物SPR1, 使用保真性较高的PrimeSTAR® HS DNA聚合酶进行ORF全长校正, PCR反应条件:98 ℃ 5 min; 98 ℃ 10 s, 56 ℃ 15 s, 72 ℃ 50 s, 33个循环; 72 ℃ 10 min。
PCR产物用1%的琼脂糖凝胶电泳检测后, 将预期大小的条带切胶回收, 连接到pMD18-T载体并转化至大肠埃希菌DH5α 感受态中, 经Amp抗性筛选和菌落PCR检测, 将含有目的基因片段的阳性克隆送公司测序。
1.2.2 LlMBF1a的生物信息学分析
用Primer Premier 5软件将目的基因的ORF序列翻译成氨基酸序列; 用EXPASY (https://www.expasy.org/tools/)中的ProtParam、SMART、SignalP、TMHMM、PSORT等工具对LlMBF1a进行生物信息学分析; 用NCBI(http://www.ncbi.nlm.nih.gov/)的BLAST功能和DNAMAN 5软件对LlMBF1a进行多重比对分析; 用MEGA 5软件构建系统进化树。
1.2.3 LlMBF1a的亚细胞定位
利用DNAMAN 5分析LlMBF1a的ORF序列的酶切位点, 结合pCAMBIA1300载体, 选用SalⅠ 和SpeⅠ 作为融合表达载体构建的酶切位点, 并设计上游特异引物SPF2和下游特异引物SPR2进行PCR扩增。双酶切pCAMBIA1300空载质粒和PCR扩增产物, 纯化酶切产物用T4连接酶连接, 获得pCAMBIA1300-LlMBF1a-GFP重组表达载体, 双酶切和测序验证连接是否成功。将构建好的载体利用冰融法转化至农杆菌GV3101中, 然后用农杆菌侵染烟草的方法[7]将构建好的pCAMBIA1300-LlMBF1a-GFP重组表达载体注射到烟草的下表皮, 空载pCAMBIA1300-GFP作为对照。暗培养1 d和光培养2 d后, 用激光共聚焦显微镜(Nikon Eclipse TE2000-E)观察和拍照, 并用Zeiss LSM Image Browser软件对照片进行分析和处理。
1.2.4 LlMBF1a的表达分析
选择生长良好、长势一致的相对抗病品种白天堂和相对感病品种粉红珍珠作为基因表达分析的材料。
LlMBF1a在不同组织中的表达:分别取常温(22 ℃)培养的白天堂的根、茎、鳞茎和叶片, 用液氮速冻并保存于-80 ℃的超低温冰箱中备用。
LlMBF1a受灰葡萄孢菌侵染的表达:将灰葡萄孢菌接种在马铃薯葡萄糖琼脂培养基(potato dextrose agar, PDA)上培养10 d, 温度25 ℃。用含有0.1% Tween 80的无菌水配成1× 106 mL-1的孢子悬浮液。采用喷雾法接种于白天堂和粉红珍珠植株上, 22 ℃保湿培养。分别在0、12、24、48、96 h取植株中部相近叶位叶片, 用液氮速冻并保存于-80 ℃的超低温冰箱中备用。
采用实时荧光定量PCR(real-time fluorescence quantitative PCR, qPCR)的方法检测基因的表达, LlMBF1a的扩增引物为qF1和qR1, 内参基因18S rRNA的扩增引物为18SqF和18SqR。参照SYBR® Premix Ex TaqTMⅡ (Tli RNaseH Plus)荧光定量试剂盒说明书进行, 仪器为Applied Biosystems Step One Plus System PCR仪。反应程序为:95 ℃ 3 min; 95 ℃ 3 s, 57 ℃ 30 s, 72 ℃ 20 s, 40个循环; 95 ℃ 15 s, 60 ℃ 1 min, 95 ℃ 15 s, 1个循环。每个样品重复3次。采用2-Δ Δ CT方法[8]分析基因的相对表达量, 用Excel软件分析数据。
获得目的基因ORF区序列长为429 bp, 编码142个氨基酸(图1)。BLAST的结果显示, 该基因与其他物种的MBF1a基因序列有较高的一致性, 暂将其命名为LlMBF1a。
ProtParam在线工具预测百合LlMBF1a蛋白包含142个氨基酸残基, 分子式为C672H1152N204O209S3, 分子量为15.53 ku。亲水性平均系数(GRAVY)为-0.713(< 0), 属于亲水蛋白, 不稳定系数为35.10(< 40), 属于稳定蛋白, 理论等电点(pI)为10.12, 属于碱性蛋白。蛋白质信号肽预测程序SignalP预测分值为0.106(< 0.5), 表明LlMBF1a不含信号肽, 不属于分泌蛋白。蛋白跨膜区域预测软件TMHMM未发现LlMBF1a有明显的跨膜区域, 蛋白质亚细胞定位工具PSORT预测LlMBF1a主要定位于细胞质或细胞核内。将LlMBF1a氨基酸序列与其他植物的MBF1a进行同源比对, 利用SMART工具分析结构, 结果表明LlMBF1a在靠近N端9~79位氨基酸残基形成1个典型的MBF1结构域(MBF1 domain), 在靠近C端86~141位氨基酸残基形成1个α 螺旋-转角-α 螺旋模序(helix-turn-helix motif, HTH motif)(图2)。
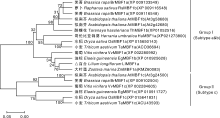
采用MEGA 5将百合LlMBF1a和其他植物的MBF1氨基酸序列构建系统进化树, 结果显示MBF1家族有2个分枝, 第Ⅰ 类MBF1(group Ⅰ ) 包括a亚型(subtype a)与b亚型(subtype b); c亚型(subtype c)与a、b亚型相似度较低, 归属第Ⅱ 类MBF1(group Ⅱ )。百合LlMBF1a归属于Ⅰ 类a亚型, 与同为单子叶植物的大叶藻(Zostera marina)的亲缘关系最近(图3), BLAST显示相似度达89%。特征结构域和系统进化分析的结果进一步说明本研究分离得到的LlMBF1a属于植物MBF1a的同源基因。
利用农杆菌侵染烟草的方法将pCAMBIA1300-LlMBF1a-GFP重组表达载体注射到烟草的下表皮, 暗培养1 d和光培养2 d后放置于激光共聚焦显微镜下观察。结果表明, 空载对照pCAMBIA1300-GFP的绿色荧光分布在细胞膜、细胞质和细胞核中。pCAMBIA1300-LlMBF1a-GFP的绿色荧光主要分布在细胞核内(图4), 表明LlMBF1a主要在细胞核中表达。
利用实时荧光定量PCR检测了LlMBF1a的表达模式。结果表明, 常温(22 ℃)条件下, LlMBF1a在百合根、茎、叶和鳞茎中均有表达, 表达量无显著差异(图5-A)。灰葡萄孢菌侵染相对抗病品种白天堂后, LlMBF1a的表达量显著上升, 在24 h达到峰值, 是对照的6.00倍, 之后有所下降, 但仍显著高于对照; 灰葡萄孢菌侵染相对感病品种粉红珍珠后, LlMBF1a的表达量显著上升, 在12 h达到峰值, 是对照的4.36倍, 之后表达量逐渐下降, 96 h时的表达量已经与对照相近(图5-B)。结果表明, LlMBF1a的表达受灰葡萄孢菌胁迫诱导, 在相对抗病品种中持续高水平表达, 说明LlMBF1a可能参与了百合对灰葡萄孢菌的防御反应。
百合灰霉病是百合的主要病害之一, 病原物为椭圆葡萄孢菌(Botrytis elliptica)[9]。我们从北京地区温室栽培的感染灰霉病的东方百合杂种系索邦植株中, 首次分离鉴定了病原物灰葡萄孢菌(Botrytis cinerea)(数据待发表), 该病原菌也能侵染麝香百合杂种系白天堂[10]。前期对百合灰霉病的研究多集中在病害发生规律及综合防治[1]、杀菌剂筛选[11, 12]和抗病种质资源[13, 14]等方面, 而百合与病原菌互作的分子机制正成为近年的研究热点。百合丝裂原活化蛋白酶MAPK基因与灰霉病抗性有关[15]。超表达岷江百合类萌发素蛋白基因LrGLP2增强了烟草对灰葡萄孢的抗性[16]。对小麦、拟南芥等的研究表明, MBF1参与了植物对病原真菌的防御反应。根据氨基酸序列的不同, 植物中的MBF1可分为a、b、c三个亚型, a亚型与b亚型相似度较高, 归属第Ⅰ 类MBF1; c亚型与a、b亚型相似度较低, 归属第Ⅱ 类MBF1[17]。本研究利用电子克隆结合RT-PCR技术从百合中分离了MBF1a基因, 序列比对及系统进化分析显示, LlMBF1a归属Ⅰ 类a亚型MBF1, 具有典型的MBF1和HTH模序。生物信息学预测LlMBF1a主要定位于细胞质或细胞核内, 进一步的亚细胞定位结果证实了LlMBF1a主要在细胞核中表达, 这与对TaMBF1a[3]、AtMBF1a[18]的研究结果一致。
组织表达模式研究表明, LlMBF1a在不同组织中表达量相当, 这与TaMBF1a[3]和AtMBF1b[17]的组织表达模式相似。TaMBF1a[3]、陆地棉GhMBF1[19]、AtMBF1a[4]、StMBF1[5]的表达均受真菌侵染诱导。番茄LeMBF1可能通过激活部分PRs基因的表达来提高植株的抗病性[20]。拟南芥过表达AtMBF1a的转基因植株, 增强了对灰葡萄孢菌的抗性[4]。在灰葡萄孢菌侵染早期, LlMBF1a的表达显著上调。与相对感病品种粉红珍珠相比, LlMBF1a在相对抗病品种白天堂中持续高水平表达, 说明LlMBF1a可能参与了百合对灰葡萄孢菌的防御反应, 但是需要进一步通过过表达和沉默方法[21]分析LlMBF1a在百合抗灰霉病方面的功能。
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|