作者简介:易可可(1994—),女,湖南岳阳人,硕士,研究方向为兽医微生物与免疫学。E-mail: kkky1024@163.com
猪伪狂犬病毒(PRV)的流行对中国养猪业造成巨大损失,而2011年后许多已免疫PRV疫苗的猪场频繁出现gE抗体转为阳性现象,感染猪出现PRV的临床症状,并出现所谓的“流产风暴”,学者们怀疑PRV的重新流行与病毒毒力增强和基因变异有关。为了解PRV变异情况,从各地疑似PRV阳性病料中,通过PK-15细胞分离出4个毒株,对毒株传代培养,进行TCID50与LD50测定,对主要毒力基因 gB、 gC、 gE和 TK进行扩增测序后分析,确定该4株病毒为PRV株,分别命名为FJ01株、FJ03株、YK株和MS2018株,滴度分别为10-6.63、10-7.08、10-8.10、10-7.18 TCID50s·0.1mL-1,对Balb/c小鼠的LD50分别为102.17、102.72、103.44、103.51 TCID50s,可见FJ01株的毒力最强。对4个毒株的毒力基因与其他PRV毒株进行同源性比对并建立进化树,FJ01株、FJ03株、MS2018株与中国近几年流行的变异毒株如HNX株、HNB株、JS-2012株等在一个大进化分支上,亲缘性较近,而与疫苗株Bartha-K61、SA215等,国际经典毒株Becker、Kaplan等亲缘性较远,变异较大。YK株与国际毒株亲缘性更近,其原因有待进一步探索。
Pseudorabies virus(PRV)’s prevalence brings huge economic losses to the domestic pig industry, however, many large-scale immunized pig herds broke out pseudorabies, and gE antybodies turned from negative to positive since 2011, causing PRV clinical symptoms infected pigs, and then resulting in “abortion storm”. Most scholars believed that national outbreak of PRV might be related to factors such as viral virulence and genetic variation. In this study, four pseudorabies viruses were successfully isolated from suspected PRV infected pigs by PK-15 cells, moreover, their TCID50 and LD50 were determined. Their main immunogenic genes and virulence-related genes gB, gC, gE and TK were amplified, sequenced and analyzed. The 4 pseudorabies viruses were affirmed, named as FJ01, FJ03, YK and MS2018 strain, respectively, whose titers were 10-6.63, 10-7.08, 10-8.10, 10-7.18 TCID50s·0.1mL-1, respectively, and the results of virulence test in Balb/c mice showed as 102.17, 102.72, 103.44, 103.51 TCID50s, respectively. The virulence of FJ01 strain was the strongest. Their nucleotide and amino acid homologies were analyzed and evolutionary trees were established. The results showed that the genes of FJ01, FJ03 and MS2018 strains had higher homology with the mutants such as HNX, HNB and JS-2012 strains which were isolated in recent years. In evolutionary relationship, they belonged to a large branch, however, they belonged to different evolutionary branches from vaccine Bartha-K61,SA215, and foreign strains Becker and Kaplan with evident variations. YK had the closer affinity with foreign strains in evolutionary relationship, but the reason remained to be further explored.
猪伪狂犬病(porcine pseudorabies, PR)是由猪伪狂犬病病毒(porcine pseudorabies virus, PRV)引起的一种由疱疹病毒感染的高度接触性传染病[1, 2], 能引起猪发热、奇痒、繁殖障碍、脑脊髓炎等症状。PRV能感染反刍动物、啮齿动物、食肉动物等哺乳动物和鸟类, 有高致病率[3, 4, 5], 但猪是PRV唯一的传播和贮存宿主[6], 能隐性感染, 长期带毒, 曾经给欧洲和美洲带来巨大经济影响[7, 8, 9, 10]。PRV主要侵害猪神经系统及生殖系统, 各个阶段猪只均可感染, 可引起妊娠母猪繁殖障碍病毒终身潜伏、流产、产死胎和呼吸道症状; 新生仔猪出现神经症状、腹泻、呕吐、生长不良等表现, 死亡率极高[11], 一旦感染该病, 难以清除[12], 其传播速度快、范围广、途径多, 国际动物卫生组织(OIE)已将其列为二类传染病[6]。20世纪gE基因缺失的Bartha-K61疫苗传入中国, 从90年代开始广泛应用于我国的各大猪场, 使PRV得到了有效的控制[13]。2011年以来, 许多接种了Bartha-K61疫苗的猪场大规模暴发PRV, 对我国养猪业和农业经济造成了巨大损失, 通过近年来的分离毒株分析, PRV变异是暴发伪狂犬病的最主要原因[14, 15]。由此可见, Bartha-K61疫苗不能对变异PRV毒株起到全面和有效保护作用[16]。
本实验从2016— 2017年疑似感染伪狂犬病的猪病料中分离出4株PRV毒株, 通过生物学特性研究分析, 并收集2011年至今的主要变异毒株和国内外经典毒株进行毒力基因gB、gC、gE和TK序列比对, 进行同源性测定并构建进化树, 分析变异株的基因间差异。
1.1.1 病料与实验动物
从福建和四川某猪场疑似PRV感染仔猪中分别采集脑、扁桃体、肺脏、脾脏等组织, -20 ℃保存备用。6周龄Balb/c小白鼠购于成都达硕实验动物有限公司。
1.1.2 主要试剂
DMEM细胞培养液、胰酶购自Hyclone公司, 胎牛血清购自AusGeneX公司; LA Taq聚合酶、T4 DNA连接酶、pMD18-T载体、GC Buffer、dNTP、大肠埃希菌DH5α 感受态细胞购自宝生物工程(大连)有限公司; 血液/组织/细胞基因组提取试剂盒购自TIANGEN生化科技有限公司; 胶回收试剂盒和质粒提取试剂盒购自OMEGA公司; 猪肾细胞(PK-15细胞)由四川农业大学微生物与免疫实验室保存。
1.2.1 病猪的病理解剖与病料处理
对采集的病猪病变组织进行研磨, 加入适量PBS制成匀浆, 反复冻融3次, 10 000 g离心5 min, 将上清液分装置于-20 ℃保存备用。
1.2.2 引物设计与合成
根据GenBank中发表的PRV gB、gC、gE、TK(登录号为KM189912.1)全基因序列, 使用Primer Premier 5.0软件设计gE检测引物和4对引物扩增该4个基因的全长, 引物序列见表1, 引物由成都擎科有限公司合成。
| 表1 引物序列信息 Table 1 Primer sequence information |
1.2.3 病毒DNA的提取
对采集的组织病料提取DNA, 使用TIANGEN的血液/组织/细胞基因组提取试剂盒, 具体操作参照试剂盒说明书。
1.2.4 病料PCR鉴定
以提取的病料DNA作为模板, 反应体系为25 μ L, LA Taq酶0.25 μ L, 2× GC Buffer Ⅰ /Ⅱ 12.5 μ L, 上下游引物各1 μ L, 模板2 μ L, dNTP 1 μ L, 灭菌去离子水补足25 μ L。鉴定PRV gE基因反应条件为94 ℃ 5 min; 94 ℃ 1 min, 61.4 ℃ 1 min, 72 ℃ 40 s, 35个循环; 72 ℃延伸10 min, 温度降至4 ℃, 加入2.5 μ L 10× Loading Buffer终止反应; 取10.0 μ L PCR产物加入1.0%琼脂糖胶孔中电泳, 于凝胶成像系统下观察结果并拍照。
1.2.5 病毒分离培养
将PCR鉴定为阳性的PRV病料处理成悬液, 4 ℃ 4 000 r· min-1离心10 min, 取上清液用0.22 μ m过滤器过滤后, 加适量双抗孵育过夜, 保存至-20 ℃。待PK-15细胞长成单层铺至80%时, 取1 mL滤液接种细胞, 轻轻混匀, 37 ℃ 5% CO2培养箱中放置1 h, 倒去滤液加入2% DMEM维持液, 同时设立对照细胞组, 每天观察细胞状况, 并记录病变情况, 待病变达到70%时收毒, 盲传5代后进行PCR鉴定。
1.2.6 病毒TCID50测定
将收集的病毒液反复冻融3次, 12 000 r· min-1离心1 min, 取上清液。PK-15细胞在96孔中培养至单层, 将分离的病毒液用DMEM培养液按10倍梯度稀释, 从10-1~10-10, 按照每个稀释度分别加1列8孔, 每孔加入100 μ L, 最后两列只加入DMEM培养液作阴性对照, 置于细胞培养箱放1 h后吸去每孔中的液体, 用PBS洗两次后加入100 μ L 2% DMEM培养液, 继续培养, 72 h后开始观察并每天记录病变孔数情况, 按Reed-Muench法计算病毒TCID50。
1.2.7 小鼠LD50测定
每株准备50只6周龄雌性SPF级Balb/c小鼠, 随机分成5组, 每组10只。将病毒10倍梯度稀释成104~100 TCID50s, 每个稀释度一组, 接种0.1 mL于小鼠大腿肌肉; 同时设立一组空白对照, 相同剂量和部位注射DMEM培养液, 在相同条件下隔离饲养。每6 h观察并记录小鼠精神状况、临床症状和死亡时间, 结果根据Reed-Muench法计算病毒对Balb/c小鼠的半数致死量(LD50)。
1.2.8 gB、gC、gE和TK全基因测序
病毒液抽提DNA后作为模板, 反应体系为50 μ L, LA Taq酶0.5 μ L, 2× GC Buffer Ⅰ /Ⅱ 25 μ L, 上下游引物各2 μ L, 模板2 μ L, dNTP 4 μ L(根据目的条带长度添加, 每1 000 bp添加1 μ L), 灭菌去离子水补足50 μ L。94 ℃ 5 min; 94 ℃ 1 min, 51 ℃(根据不同引物选择退火温度)1 min, 72 ℃ 1 min(根据目的条带大小选择, 每1 000 bp延长1 min), 35个循环; 72 ℃延伸10 min, 温度降至4 ℃, PCR产物加入1.0%琼脂糖胶孔中电泳, 回收目的片段, 连接pMD18-T载体转入大肠埃希菌DH5α 感受态细胞, 在LB氨苄固体培养基上筛选出阳性菌后, 提取质粒, 送往成都擎科生物有限公司测序。
1.2.9 毒力基因全基因序列分析
参考多株国内外经典和变异PRV毒株, 利用Mega7.0和MegAlign软件将测序结果的gB、gC、gE和TK基因序列进行对比和建立进化树。
2.1.1 病理剖检结果
患病仔猪剖检后发现所有仔猪均出现脑出血, 扁桃体坏死, 肺脏和肾脏有出血点, 肝脏和肺脏表面有白色坏死灶等症状。
2.1.2 病料检测结果
病料组织进行gE基因PCR扩增后, 在检测的脑部、扁桃体、肾脏、肺脏等均扩增出553 bp的目的条带。
2.1.3 病毒的分离
处理的组织悬液接种到长满单层的PK-15细胞上, 第1代均出现病变, 盲传几代后时间和CPE稳定, 接毒后24 h后细胞变圆变亮, 聚集, 拉网并形成合胞体(图1-A), 而对照组没有病变(图1-B)。
 | 图1 病料悬液上清液感染PK-15细胞病变图(100× ) A, PRV感染细胞; B, 正常细胞对照。Fig.1 Cytopathic effect of PK-15 cells infected by epidemic tissue suspension supernatant (100× ) A, Virus infected cell; B, Normal cell control. |
2.1.4 病毒液的PCR鉴定
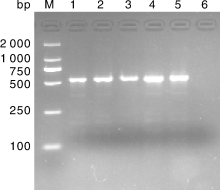
对病毒液提取的核酸进行PRV gE PCR鉴定, 结果能扩增出目的条带(图2)。
2.1.5 病毒滴度测定
病毒在PK-15细胞上传第1代和第5代的都收毒进行滴度测定, 按照Reed-Muench法计算PRV的滴度, 单位为每0.1 mL病毒液中含多少TCID50s的病毒粒子, 结果如表2。
| 表2 不同代次PRV毒株滴度测定 Table 2 Titers identification of different passage PRV strains |
2.1.6 小鼠LD50测定
PRV FJ01株、FJ03株、YK株和MS2018株分别攻毒Balb/c小鼠后, 临床症状为局部严重瘙痒、呼吸急促、被毛蓬乱、频繁舔咬注射部位并裸露出皮肤, 死亡时间平均为54~96 h, 高剂量小鼠全部死亡, 对照组小鼠精神状态正常。PRV各毒株对Balb/c小鼠的半数致死量LD50分别为102.17、102.72、103.44、103.51 TCID50s(表3)。
| 表3 PRV毒株对Bablb/c小鼠LD50测定 Table 3 LD50 measurement of PRV strains on Balb/c mice |
2.2.1 gB基因
PRV FJ01株、PRV FJ03株、PRV YK株和PRV MS2018株的gB基因核苷酸序列与2011年以来国内流行的PRV变异株HNB、ZJ01、JS-2012、TJ株等的同源性为98.5%~100%, 与疫苗株Ea、Fa和Bartha株同源性为98.2%~99.8%, 与国内外PRV经典毒株Kaplan、Kolchis、NIA3、Becker等同源性为97.7%~99.6%; 4个分离PRV毒株的gB基因编码的氨基酸与近年流行的变异株同源性为97.0%~100%, 与疫苗株同源性为96.3%~99.7%, 与经典毒株同源性为95.3%~99.1%。PRV FJ01、FJ03和MS2018株在进化树上与近几年国内分离的PRV变异株HN1201、HNX、HNB等在同一大分支; YK株与国外经典毒株亲缘性更近(图3-A)。
 | 图3 PRV分离株gB、gC基因的核苷酸遗传进化树Fig.3 Phylogenetic tree of PRV gB and gC gene between PRV strains and other reference strains |
2.2.2 gC基因
PRV FJ01株、FJ03株和MS2018株gC基因的核苷酸序列与近年流行变异PRV株同源性为91.8%~99.9%, 与Ea、Fa、Bartha和SA215疫苗株同源性为91.9%~99.9%, 与国内外经典毒株同源性为89.3%~98.7%, 同源性较低; gC基因编码的氨基酸与变异毒株, 除YK株外同源性为97.0%~100%, YK株为89.5%~89.7%, 同源性较低; 与PRV疫苗株同源性为88.4%~99.4%, 与国内外经典毒株同源性为86.0%~96.9%。在进化分支上, PRV FJ01株、FJ03株、MS2018株与国内毒株亲缘性更近, 与近年的变异株在同一大进化分支上, 而YK株与国外经典毒株在同一进化分支上, 与国内毒株亲缘性远(图3-B)。
2.2.3 gE基因
PRV FJ01株、F0J3株和MS2018株gE基因的核苷酸序列与近年流行变异PRV株同源性为95.9%~99.5%, 与Ea、Fa、Bartha疫苗株的同源性为96.4%~99.5%, 与Kaplan、Becker、Kolchis、Hercules等国外经典毒株同源性为96.1%~98.8%; gE基因编码的氨基酸与近年变异PRV株同源性为90.6%~100%; 与疫苗毒株同源性为95.8%~99.4%, 与国外经典毒株同源性为95.6%~100%。FJ01株、FJ03株、MS2018株在进化树上与国内2011年后分离出的PRV毒株如HNX株、HLJ8株、HB1201株、HN1201株等在同一大进化分支上, 与疫苗毒株和国内外经典毒株亲缘性较远; YK株与国外经典毒株在同一进化分支上, 亲缘性较近(图4-A)。
 | 图4 PRV分离株gE、TK基因的核苷酸遗传进化树2.2.4 TK基因Fig.4 Phylogenetic tree of PRV gE and TK gene between PRV strains and other reference strains |
4个分离PRV毒株的TK基因核苷酸序列与国内近几年流行分离HNX、JS-1201、HB1201、BJ/YT等变异毒株同源性为98.4%~100%, 与Bartha、Fa、Ea等疫苗株同源性为98.6%~100%, 与国外经典毒株Kaplan、Becker等同源性在97.9%~99.7%, 各毒株间遗传变异不大, 同源性都很高, 说明TK基因较为保守。TK编码的氨基酸序列与近年变异株同源性为99.7%~100%, 与疫苗株同源性为99.0%~99.9%, 与国外经典毒株同源性为98.3%~99.9%, 同源性较高。FJ01株、FJ03株与MS2018株的TK基因序列在进化树上与国内分离的各PRV毒株在同一进化分支上, 与国内毒株亲缘性较近; YK株的TK基因与国内和国外均亲缘性较远, 在单独一个分支上(图4-B)。
自2011年以来, 中国许多地区免疫过Bartha-K61疫苗的猪场大规模暴发PRV[17], 且在国内广泛流行, 有研究已经确定了是由PRV变异毒株引起[18], 意味着Bartha-K61疫苗已不能全面提供保护[19], 疑似暴发PRV猪场的猪表现为高烧、严重呼吸道疾病、厌食、震颤等精神症状[18]。本研究对各地猪场有疑似PRV的病料进行抗原检测和病毒分离, 得到4株PRV病毒, 初步鉴定为野毒感染, 并深入研究是否为变异毒株以及生物学特性探究。
本实验采用猪肾PK-15细胞分离病毒, 4个病毒分别命名为PRV FJ01株、PRV FJ03株、PRV YK株和PRV MS2018株。将病毒盲传至5代, 同时与第一代病毒做TCID50, 发现滴度随着代数增多而增加。用第5代毒攻毒Balb/c小鼠计算半数致死量, 毒力最强的毒株为PRV FJ01株, LD50为102.17 TCID50s· 0.1mL-1, 而我国在2011年前就分离得到的Fa、Ea和S经典毒株LD50分别是100.7、102.0和103.83 TCID50s, 2011年后分离出的HNX、HNB、TJ、HeN1和JS-2012株的LD50分别为102.0、102.4、102.3、102.37和102.37 TCID50s, 可以看出Fa毒力是最高的, 由此可以得知, 中国变异株的毒力没有增强, 猪群暴发伪狂犬病且高死亡率与毒力增强无关, 但从小鼠实验结果可以发现, 变异株能让小鼠产生更为严重的瘙痒症状。
gB是PRV必需糖蛋白, 也是主要的免疫相关蛋白, 是最保守的蛋白之一, 是病毒感染所必需的, 与病毒入侵细胞和在细胞间传播密切相关[20], 产生中和病毒的抗体[21]。gC参与病毒入侵细胞过程, 是PRV最主要的保护性抗原之一, 能诱导细胞免疫, 产生中和抗体[19], gB和gC的变异性, 是伪狂犬病毒的特征; gE不是病毒复制必需的蛋白, 但它是主要的毒力因子之一, 呈现出嗜神经性, 在病毒释放与传播中使PRV接触临近的神经元, 从而进入中枢神经系统, 促进病毒在内转运和扩散[22], 有研究表明, gE缺失株与其他蛋白缺失株相比亲神经性更弱, 因此gE可能在侵蚀和传播神经系统中有更重要的作用[23]。TK也是主要毒力基因, 与建立和激活神经潜伏状态, 在中枢神经中增殖有关[24], 当缺失TK时, 病毒增殖不受到影响, 但毒力和侵染力大幅度降低[25], 因此在基因缺失苗研发中常使用缺失TK的PRV毒株。通过gB、gC、gE和TK全基因的遗传进化分析建立进化树, PRV FJ01株、PRV FJ03株和PRV MS2018株与2011年后分离的变异株亲缘性相近, 而YK株与国外毒株在同一进化分支上, 与国内毒株亲缘性较远。4株分离PRV的gB核苷酸序列与国内外PRV参考株的同源性为97.7%~100%; gC核苷酸序列与国内外PRV的同源性为89.3%~99.9%; gE与国内外PRV的核苷酸同源性为96.1%~99.8%; TK基因与国内外PRV的核苷酸同源性为97.9%~100%。分析各个毒株分别与2011年至今流行的PRV的毒力基因同源性, 发现同源性较高, 说明2011后的流行毒株间变异较小。
通过分离出来的4个毒株与国内市面上主要流通的疫苗毒株如Bartha-K61株和SA215株进行基因序列比对有一些变异, 虽然目前流行病学数据显示我国猪场加强疫苗免疫可以大部分防控PRV, 但不能完全清除, 这与我国还有许多散户, 养殖环境等有关, 这可能也是PRV仍在流行变异的原因之一[26]。为了防控新变异PRV, 以近年流行的PRV为亲本研发新型疫苗可能对猪起免疫保护作用更加有效; 且随着全基因组测序的普及, 关于PRV遗传变异的研究越来越多, 数据库越来越大, 发现PRV虽然GC含量高, 结构稳定, 但仍出现变异, YK毒株分离于近年感染伪狂犬病的病料, 其免疫原性基因gB、gC和gE与国外毒株相近, TK在进化树上位于独立分支上, TK毒株是否出现基因重组, 需要从全基因组角度来进行进一步探究。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|